理解特应性皮炎与肠道微生物群之间的联系
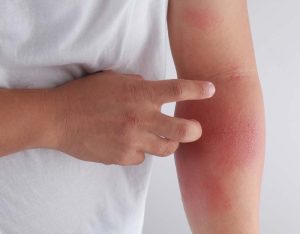
特应性皮炎,也被称为湿疹,是一种炎症性皮肤病,会导致皮肤发红、发炎和瘙痒。这种病症的症状可能非常折磨人,持续的瘙痒和皮肤不适会导致睡眠障碍,甚至引发焦虑和抑郁(1) 特应性皮炎是一种常见疾病,通常在儿童时期发病,全球约 2% 的成年人和 4% 的儿童受其影响(2) 虽然其确切病因尚不清楚,但研究人员认为遗传和环境因素都在其病因中起作用。有趣的是,患有特应性皮炎的人通常有此病或其他过敏性疾病(如哮喘和花粉症)的家族史。这表明这些人可能具有遗传易感性,而疾病的发生或进展可能受到空气污染物、过敏原、感染、气候和压力等环境因素的触发。
特应性皮炎与肠道健康之间有联系吗?
我们皮肤和肠道内的微生物持续相互作用和影响,形成了所谓的“肠-皮轴”。这种联系表明,了解肠道微生物群对于有效管理湿疹等皮肤病至关重要。 研究表明,肠道微生物群的组成和多样性与特应性皮炎的发生发展之间存在令人兴奋的关联(3) 事实上,肠道微生物群的变化可以早在婴儿期就发生,而这些变化可以决定特应性皮炎的严重程度(4)
 2018 年发表的一篇综述文章指出,特应性皮炎患者通常肠道微生物群的整体多样性较低,并且某些细菌(如 Clostridia、Clostridium difficile、Escherichia coli 和 Staphylococcus aureus)的丰度高于健康对照组。相反,益生菌(如 Bifidobacteria、Bacteroidetes 和 Bacteroides)的含量在这些患者中较低(5) 同样,2021 年的一篇综述文章指出,特应性皮炎患者的肠道微生物群组成受到干扰,其中 Faecalibacterium prausnitzii、Clostridium 的水平增加,而婴儿患者中 Escherichia 水平升高,同时 Akkermansia、Bacteroidetes 和 Bifidobacterium 的水平降低(6) 此外,研究表明,患有特应性皮炎的婴儿体内 Faecalibacterium、Oscillospira、Bacteroides、Parabacteroides 和 Sutterella 水平升高,而短链脂肪酸(SCFA)产生菌(如 Bifidobacterium、Blautia 和 Eubacterium)的水平下降(7) 一项针对 132 名受试者(其中 90 名为特应性皮炎患者)的研究发现,某种特定亚种的 Faecalibacterium prausnitzii 在患者的粪便样本中过量存在。这些细菌会产生 SCFA,具有抗炎作用。这种减少似乎是由于 F. prausnitzii 菌群的变化,其中富含产丁酸的菌株减少。此外,特应性皮炎患者的肠道微生物群表现出富集的基因,这些基因帮助细菌利用受损肠道释放的营养物质。这表明,特应性皮炎引起的肠道炎症可能为某些细菌创造了适宜的生存环境,进一步加剧了问题。
2018 年发表的一篇综述文章指出,特应性皮炎患者通常肠道微生物群的整体多样性较低,并且某些细菌(如 Clostridia、Clostridium difficile、Escherichia coli 和 Staphylococcus aureus)的丰度高于健康对照组。相反,益生菌(如 Bifidobacteria、Bacteroidetes 和 Bacteroides)的含量在这些患者中较低(5) 同样,2021 年的一篇综述文章指出,特应性皮炎患者的肠道微生物群组成受到干扰,其中 Faecalibacterium prausnitzii、Clostridium 的水平增加,而婴儿患者中 Escherichia 水平升高,同时 Akkermansia、Bacteroidetes 和 Bifidobacterium 的水平降低(6) 此外,研究表明,患有特应性皮炎的婴儿体内 Faecalibacterium、Oscillospira、Bacteroides、Parabacteroides 和 Sutterella 水平升高,而短链脂肪酸(SCFA)产生菌(如 Bifidobacterium、Blautia 和 Eubacterium)的水平下降(7) 一项针对 132 名受试者(其中 90 名为特应性皮炎患者)的研究发现,某种特定亚种的 Faecalibacterium prausnitzii 在患者的粪便样本中过量存在。这些细菌会产生 SCFA,具有抗炎作用。这种减少似乎是由于 F. prausnitzii 菌群的变化,其中富含产丁酸的菌株减少。此外,特应性皮炎患者的肠道微生物群表现出富集的基因,这些基因帮助细菌利用受损肠道释放的营养物质。这表明,特应性皮炎引起的肠道炎症可能为某些细菌创造了适宜的生存环境,进一步加剧了问题。
该领域的现有证据表明,特应性皮炎患者肠道微生物群整体组成的变化可能会导致肠道上皮屏障受损,并对过敏原和其他环境因素的免疫反应改变,这两者都可能促进特应性皮炎的进展。
我们能通过调节微生物群来管理湿疹吗?
 关于肠道-皮肤轴及其对特应性皮炎影响的新兴证据,为管理这种皮肤病的创新策略提供了令人兴奋的可能性。通过饮食干预、益生元、益生菌或其他方法调节肠道微生物群,可能是管理湿疹症状并改善患者生活质量的关键。通过改善肠道微生物群的平衡,我们可以减少全身炎症,加强和支持皮肤的天然屏障功能,修复肠道通透性并调节免疫系统,所有这些都是管理特应性皮炎的重要因素。
关于肠道-皮肤轴及其对特应性皮炎影响的新兴证据,为管理这种皮肤病的创新策略提供了令人兴奋的可能性。通过饮食干预、益生元、益生菌或其他方法调节肠道微生物群,可能是管理湿疹症状并改善患者生活质量的关键。通过改善肠道微生物群的平衡,我们可以减少全身炎症,加强和支持皮肤的天然屏障功能,修复肠道通透性并调节免疫系统,所有这些都是管理特应性皮炎的重要因素。
值得注意的是,有证据表明,通过各种方法靶向肠道微生物群可能是成功的。例如,一项包含 1,382 名特应性皮炎患者、涉及 25 项随机对照试验的荟萃分析表明,益生菌可能有助于减少湿疹症状。(9) 益生菌对轻度或中度湿疹患者、服用时间超过三个月的患者以及使用含有特定益生菌菌株乳酸菌 (Lactobacillus)的患者效果最佳。与此同时,一项使用小鼠模型的研究表明,针灸治疗可以显著改变肠道微生物结构并改善肠道屏障功能,从而改善特应性皮炎症状。(10)
利用 Enbiosis AI 驱动的微生物群分析管理特应性皮炎
Enbiosis 提供了一种创新方法,帮助您深入了解自己独特的肠道微生物群概况。我们最先进的 AI 驱动肠道微生物群分析提供个性化的食物和补充剂建议,旨在优化肠道健康,并从根本上解决特应性皮炎等问题。多项临床研究支持,我们的 AI 分析已被证明可以改善症状,提高生活质量,并在 IBS(肠易激综合征)和功能性便秘患者中促进肠道微生物群多样性的显著变化。(10,11,12) 通过将相同的数据驱动方法应用于特应性皮炎,我们帮助恢复微生物平衡,减少炎症,并加强皮肤屏障。理解肠道-皮肤连接,为有针对性、科学支持的解决方案打开了大门。Enbiosis 通过个性化营养策略赋予您支持长期皮肤健康的能力。立即开始您的健康皮肤之旅,因为真正的健康始于肠道。
了解更多
参考文献:
1 Schonmann, Y., Mansfield, K. E., Hayes, J. F., Abuabara, K., Roberts, A., Smeeth, L., & Langan, S. M. (2020). 成年特应性湿疹与抑郁和焦虑风险:一项基于人群的队列研究。 《过敏与临床免疫学杂志:实践》, 8(1), 248.
2 Tian, J., Zhang, D., Yang, Y., Huang, Y., Wang, L., Yao, X., & Lu, Q. (2023). 特应性皮炎的全球流行病学:一项全面的系统分析和建模研究。 《英国皮肤病学杂志》, 190(1), 55–61.
3 Pessemier, B. D., Grine, L., Debaere, M., Maes, A., Paetzold, B., & Callewaert, C. (2021). 肠道-皮肤轴:微生物失调与皮肤疾病之间相互关系的当前认知。 《微生物学》, 9(2), 353.
4 Liu, X., Cai, M., Chen, M., Chen, J., Zhu, T., Wu, S., & Jia, J. (2024). 婴儿特应性皮炎严重程度与肠道微生物群变化的关联。 《澳大利亚皮肤病学杂志》, 65(4), 328–336.
5 Lee, S. Y., Lee, E., Park, Y. M., & Hong, S. J. (2018). 特应性皮炎中的肠道-皮肤轴微生物组。 《过敏、哮喘与免疫研究》, 10(4), 354-362.
6 Pessemier, B. D., Grine, L., Debaere, M., Maes, A., Paetzold, B., & Callewaert, C. (2021). 肠道-皮肤轴:微生物失调与皮肤疾病之间相互关系的当前认知。 《微生物学》, 9(2), 353.
7 Reddel, S., Chierico, F. D., Quagliariello, A., Giancristoforo, S., Vernocchi, P., Russo, A., Fiocchi, A., Rossi, P., Putignani, L., & Hachem, M. E. (2019). 特应性皮炎儿童的肠道微生物群特征及益生菌混合物的肠道持久性评估。 《科学报告》, 9, 4996.
8 Song, H., et al. (2016). 人类肠道微生物组中特应性皮炎相关的屎肠球菌亚种失调。 《过敏与临床免疫学杂志》, 137(3), 852-860.9 Kim, K., Lee, E., Kim, M., Lee, K. S., Sol, I. S., Min, T. K., Yang, H. J., & Hong, S. J. (2023). 益生菌治疗特应性皮炎的疗效:随机对照试验的系统评价和亚组分析的荟萃分析。 《亚太过敏与免疫学杂志》, 10.12932/AP-280323-1576. 在线发表.
10 Yeom, M., Ahn, S., Hahm, D., Jang, S., Jang, S. H., Park, S., Jang, J., Park, J., Oh, J., Lee, I., Kim, K., Kwon, S., & Park, H. (2024). 针灸通过调节肠道屏障功能改善小鼠特应性皮炎,该作用依赖于肠道微生物群。 《综合医学杂志》, 22(5), 600-613.
11 Tunali, V., Arslan, N. Ç., Ermiş, B. H., Derviş Hakim, G., Gündoğdu, A., Hora, M., & Nalbantoğlu, Ö. U. (2024). 以微生物组为基础的人工智能辅助个性化饮食 vs 低发酵寡糖、二糖、单糖和多元醇饮食:管理肠易激综合征的新方法的多中心随机对照试验。 《美国胃肠病学杂志》, 119(9), 1901-1912.
12 Arslan, N. Ç., Gündoğdu, A., Tunali, V., Topgül, O. H., Beyazgül, D., & Nalbantoğlu, Ö. U. (2022). 人工智能辅助个性化微生物组调节饮食治疗功能性便秘的疗效:一项随机对照试验。 《临床医学杂志》, 11(22), 6612.